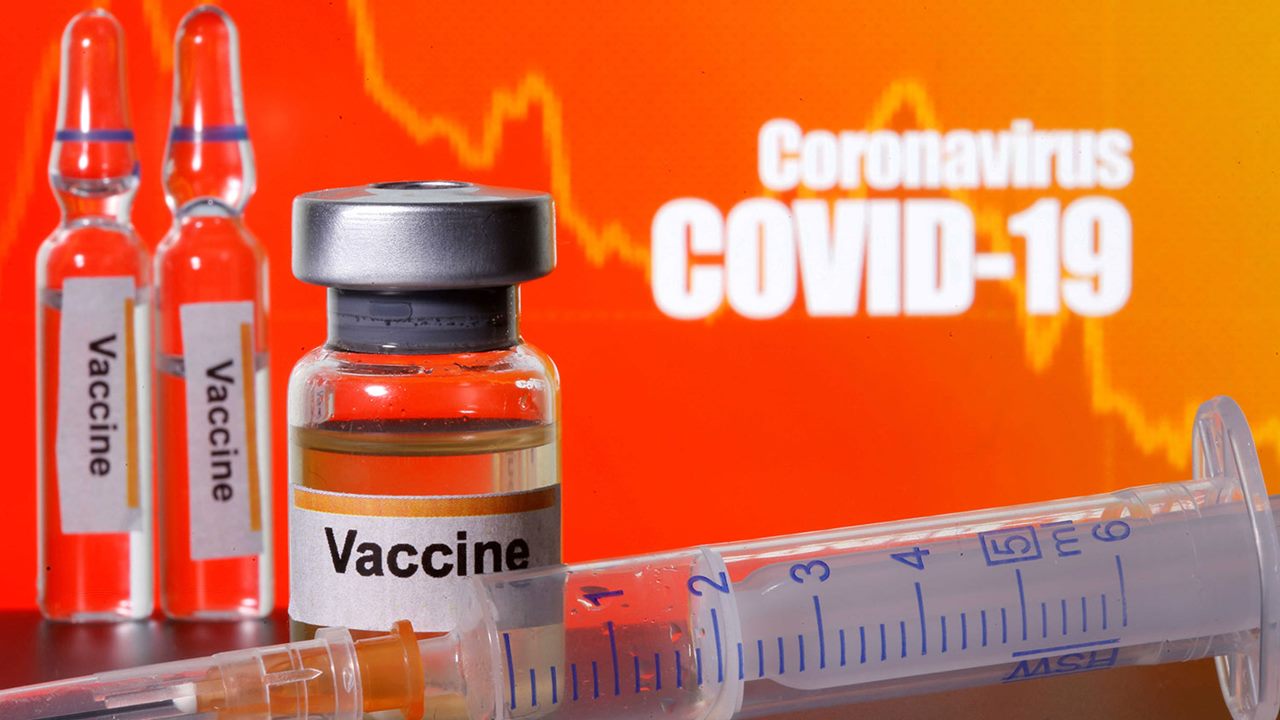
VACUNA CONTRA COVID 19 DE MODERNA ES EFICAZ EN UN 94.5%,SEGÚN ESTUDIOS
CIUDAD DE MÉXICO,16 noviembre 2020/REDACCIÓN EL FINANCIERO/
Moderna dijo que su vacuna contra el COVID-19 fue 94.5 por ciento efectiva en un análisis preliminar de un gran ensayo clínico en etapa tardía, otra señal de que una búsqueda acelerada por parte de científicos y compañías farmacéuticas está dando sus frutos con nuevas herramientas potentes que podrían ayudar a controlar la pandemia.
La lectura altamente positiva se produce solo una semana después de que se descubrió que una inyección similar desarrollada por Pfizer y BioNTech era más del 90 por ciento efectiva en un análisis intermedio.
Ambas inyecciones se basan en una tecnología llamada ARN mensajero que nunca se ha utilizado para fabricar una vacuna aprobada.
Un análisis preliminar de datos de más de 30 mil voluntarios mostró que la vacuna de Moderna previno prácticamente todos los casos sintomáticos de COVID-19, la enfermedad causada por el coronavirus, dijo la compañía en un comunicado este lunes.
Las acciones de Moderna subieron un 12 por ciento en las operaciones previas a la comercialización en EU, mientras que en Europa, el índice Stoxx 600 subió un 1.4 por ciento. El repunte de las acciones globales tras la noticia representó alrededor de 120 mil millones en valor de mercado agregado al índice MSCI All Country World.
Solo cinco participantes que recibieron dos dosis de la vacuna se enfermaron, en comparación con 90 casos de coronavirus en los participantes que recibieron un placebo, según una revisión realizada por una junta de monitoreo de seguridad de datos independiente designada por los Institutos Nacionales de Salud de EU.
La vacuna también pareció ser eficaz para prevenir las infecciones más graves por COVID-19. No hubo casos graves entre las personas que recibieron la vacuna, en comparación con 11 en los voluntarios que recibieron inyecciones de placebo, según la declaración de Moderna.
Los resultados llegan en un momento en el que el control de la pandemia se está intensificando. Estados Unidos superó los 11 millones de casos de coronavirus el domingo, ya que Florida reportó la mayor cantidad de infecciones nuevas desde julio y los nuevos casos en California alcanzaron un máximo de tres meses. También aumentan las muertes y las hospitalizaciones. Europa también ha visto cómo los casos se han disparado a medida que gran parte del mundo se prepara para lo que se espera sea un invierno terrible.
Si bien los resultados son preliminares, se espera que tanto Moderna como Pfizer soliciten la autorización de uso de emergencia de la Administración de Alimentos y Medicamentos de EU, si un estudio adicional muestra que sus vacunas son seguras. En su comunicado, Moderna dijo que podría buscar el visto bueno de los reguladores en las próximas semanas.
La compañía dijo que esperaría que una autorización de emergencia se base en un análisis final que contenga 151 casos, junto con dos meses de datos de seguimiento de seguridad que los reguladores estadounidenses quieren ver. Se espera que los datos finales a finales de este mes.
Moderna, con sede en Cambridge, Massachusetts, recibió 955 millones de dólares del programa Operation Warp Speed de EU para desarrollar su vacuna, y Estados Unidos acordó pagar hasta 1.53 mil millones para comprar el suministro de la inyección. Pfizer ha dicho que no recibió ningún financiamiento federal para desarrollar su vacuna, aunque llegó a un acuerdo de suministro con Estados Unidos por valor de casi 2 mil millones de dólares.
Esto es lo que sabemos de la vacuna de Moderna, una nueva esperanza contra la pandemia
La compañía estadounidense usa ARN mensajero dentro de las células para producir una reacción inmunológica
El mRNA-1273 de Moderna consiste en una hebra de mRNA que le dice al cuerpo que produzca la proteína de pico que el coronavirus usa para adherirse a las células humanas.
La hebra es como un lado de una cremallera; los ‘dientes’ son una secuencia de letras químicas que las células leen para producir los mil 273 aminoácidos que componen la proteína de pico. Si la vacuna funciona según lo previsto, el cuerpo comenzará a producir las proteínas poco después de la inyección, lo que provocará que el sistema inmunológico reaccione y acumule anticuerpos protectores contra ellas.
Las grandes ventajas de las vacunas de ARNm son la rapidez y la flexibilidad. No se necesitan células vivas meticulosas o virus difíciles de manejar, y la química básica es sencilla.
La vacuna de Moderna llegó a los ensayos en humanos de fase I el 16 de marzo, solo 63 días después de que la compañía comenzara a desarrollarla. Y el 27 de julio, el primer voluntario en la prueba de eficacia en etapa final de 30 mil personas de Moderna en EU recibió una inyección. Menos de 12 horas después, BioNTech y su socio, Pfizer, dijeron que ellos también estaban comenzando una prueba, un estudio que se llevará a cabo en Estados Unidos, Brasil y varios otros países.
En los ensayos de Fase I, las vacunas Moderna y BioNTech-Pfizer estimularon el sistema inmunológico de las personas para producir anticuerpos que neutralizaron el virus en experimentos de laboratorio, un signo inicial positivo.
«Esta es una plataforma relativamente nueva, pero se ve bastante bien», dijo Anthony Fauci , director del Instituto Nacional de Alergias y Enfermedades Infecciosas, después de que se publicaran los resultados del ensayo de Fase I de Moderna, patrocinado por NIAID. «Los anticuerpos neutralizantes son el estándar de oro de protección». Moderna, que ha trabajado con NIAID durante años, está recibiendo 955 millones de dólares del Gobierno de EU para respaldar sus ensayos de coronavirus.
Se desconoce qué tan bien las vacunas de ARNm evitarán la COVID-19. Ninguna vacuna basada en ARN mensajero ha sido aprobada para ninguna enfermedad, ni siquiera ha entrado en ensayos de etapa final hasta ahora, por lo que hay pocos datos humanos publicados para comparar el ARNm con tecnologías más antiguas.
En el ensayo de Fase I de Moderna, los 15 pacientes que recibieron la mediana de tres tamaños de dosis informaron al menos un efecto secundario, aunque ninguno fue grave. Tres de los 15 pacientes que recibieron la dosis más alta tuvieron reacciones graves temporales. Esa dosis no se probará más.
La posibilidad de una inyección de COVID-19 ha llevado a los inversores a triplicar el valor de las acciones de Moderna este año, lo que le dio a la empresa una capitalización de mercado de alrededor de 28 mil millones de dólares, una cifra asombrosa para una empresa sin producto.
Moderna recibió 955 millones de dólares del programa Operation Warp Speed de Estados Unidos. Estados Unidos acordó pagar hasta 1.53 mil millones de dólares para comprar suministros de la toma Moderna.
Una vez que se aprueben las vacunas, el esfuerzo por inmunizar a cientos de millones de personas deberá superar una serie de obstáculos. El almacenamiento y distribución de algunos de los productos es complejo. La vacuna de Pfizer debe almacenarse ultra fría hasta unos días antes de su uso, pero puede mantenerse a temperatura del refrigerador hasta por cinco días. Moderna, por su parte, señaló nuevos datos que muestran que su vacuna es estable a la temperatura del refrigerador durante 30 días, mucho más que los siete días estimados anteriormente. Puede conservarse en congeladores durante un período más largo y no necesita las instalaciones especiales requeridas para la vacuna Pfizer.
Moderna ya ha llegado a acuerdos para suministrar 100 millones de dosis a Estados Unidos y 80 millones a la Unión Europea, entre otros. El Reino Unido dijo el lunes que está negociando con la compañía, pero que ninguna dosis estará disponible en el país hasta la próxima primavera, como muy pronto.
Los resultados son preliminares, pero se espera que tanto Moderna como Pfizer soliciten la autorización de uso de emergencia de la Administración de Drogas y Alimentos de EU si una revisión adicional demuestra que sus vacunas son seguras. Moderna dijo que podría solicitar la autorización de los reguladores.